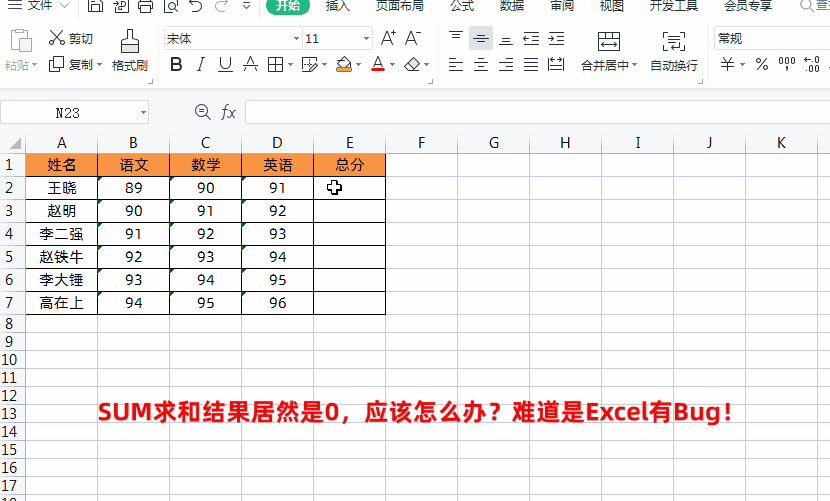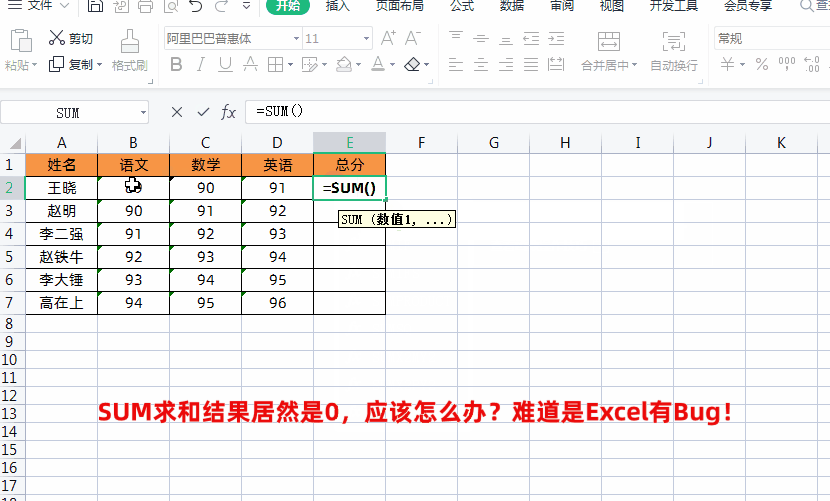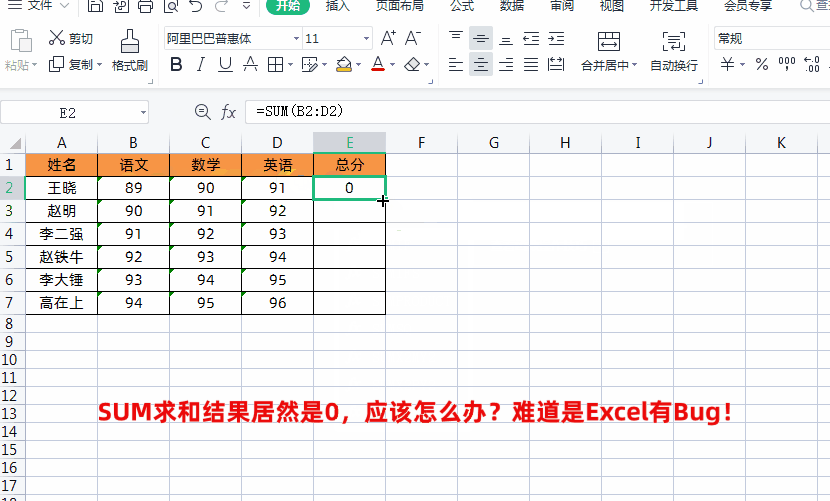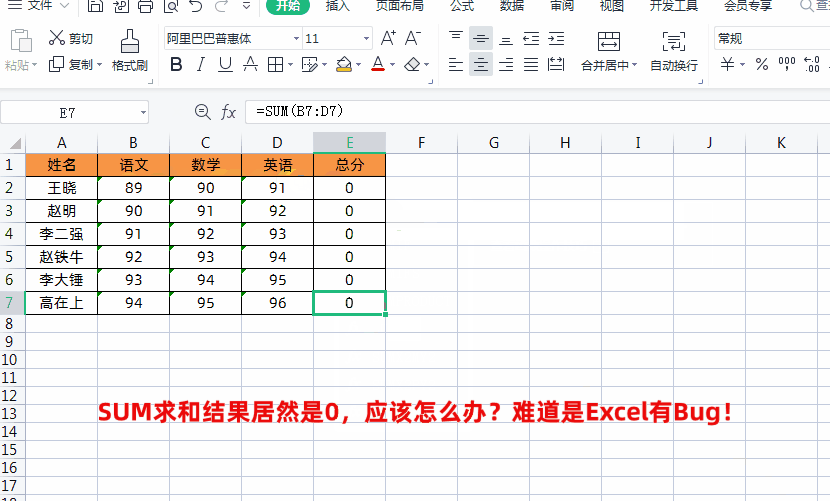
我是【桃大喵学习记】,点击右上方“关注”,每天为你分享职场办公软件使用技巧干货!我们在日常工作中有时会遇到这样的情况,我们对Excel表格数据进行求和时,结果竟然是0,很多小伙伴甚至都怀疑是不是Excel有Bug!其实,在WPS的Excel表格中数据求和,结果为0无法正确求和的的主要原因是:表格数值的格式是文本格式,因为文本格式下的数值相当于字母或汉字,当然无法进行求和。
那么,遇到这种求和问题应该如何解决呢?
方法1使用减负运算求和通过两个减号“--”,把文本格式数字转换成数值,我们可以通过在求和公式里面的第一个单元格前面加两个减号“--”,也就是减负运算,把表格中的文本格式数字转换成数值格式,然后再进行求和运算就可以了。
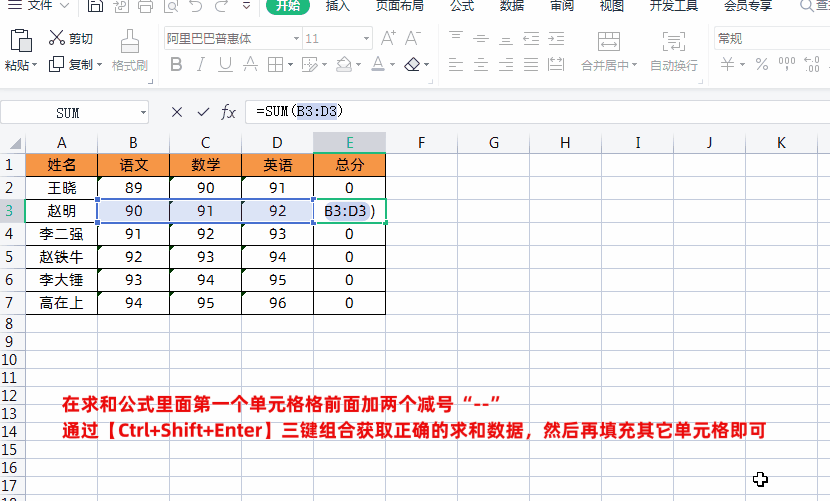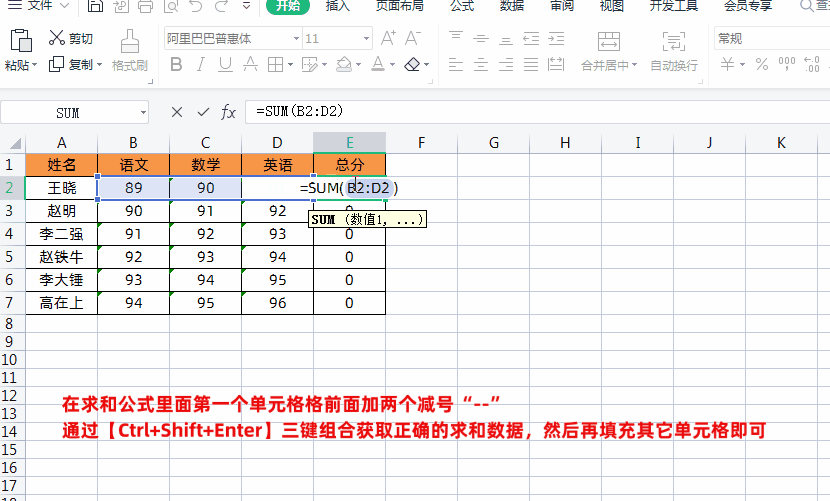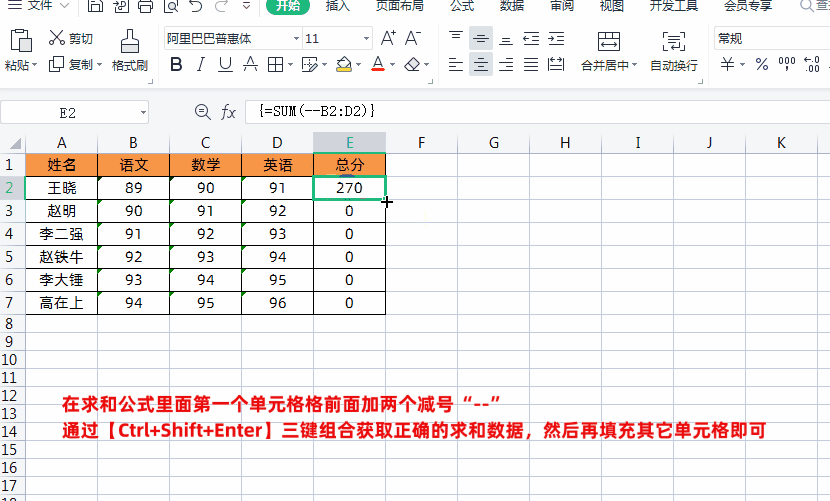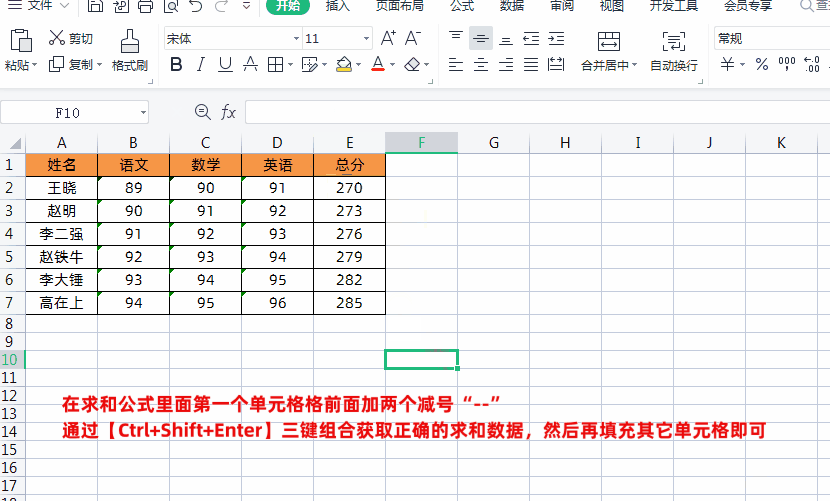
1、首先在求和公式里面第一个单元格格前面加两个减号“--”,如下图所示
2、然后再通过按【Ctrl+Shift+Enter】三键组合,这样就可以获取正确的求和数据了,然后再填充其它单元格即可,如下图所示
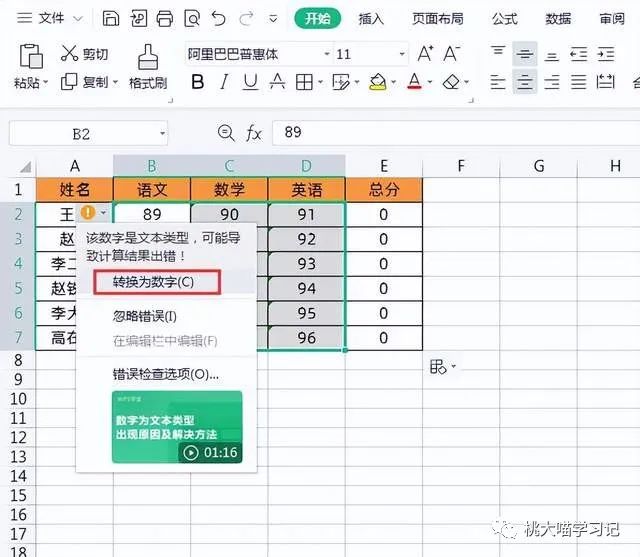
方法2把文本数字转换成数值后求和我们可以全选表格所有文本数字,然后左上角会有一个黄色的“叹号”,点击“叹号”下拉菜单→点击【转换为数字】即可,如下图所示

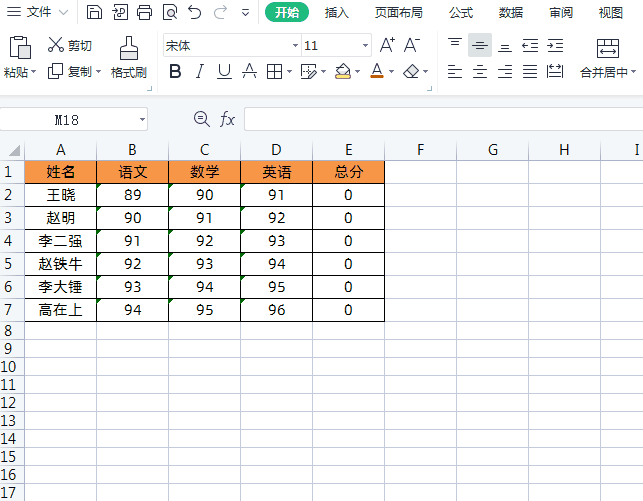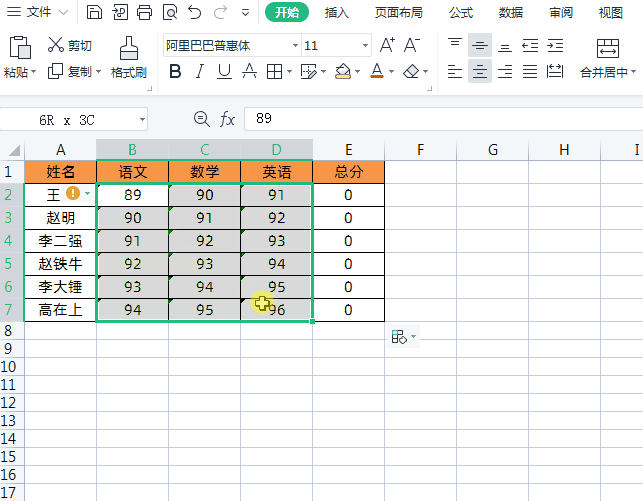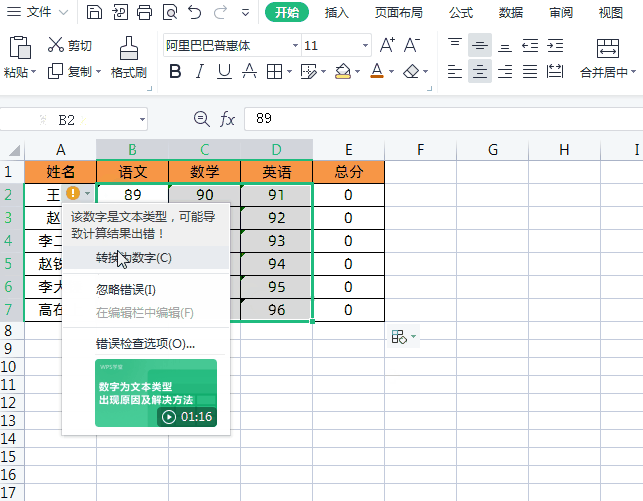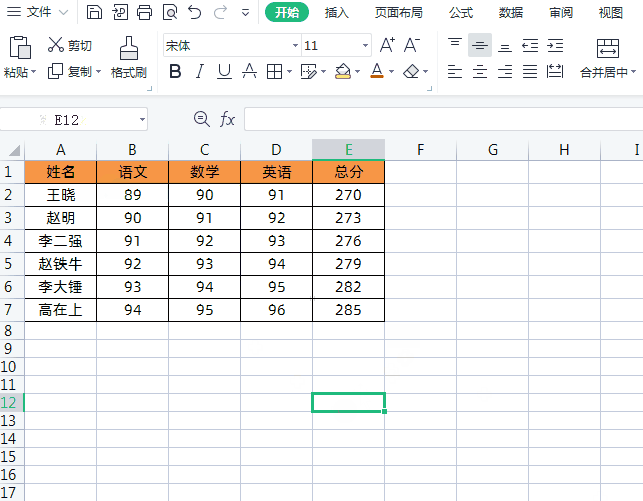
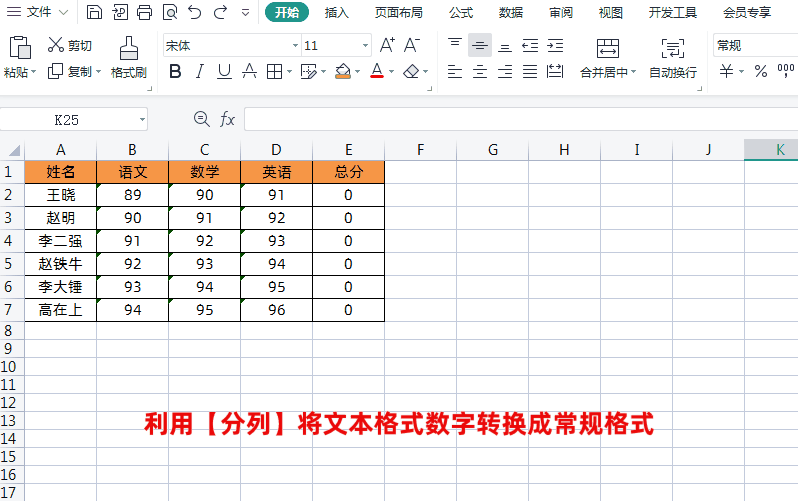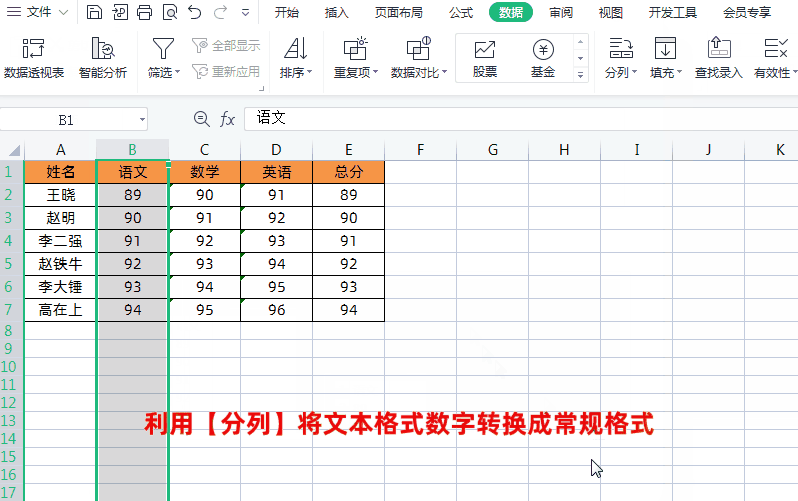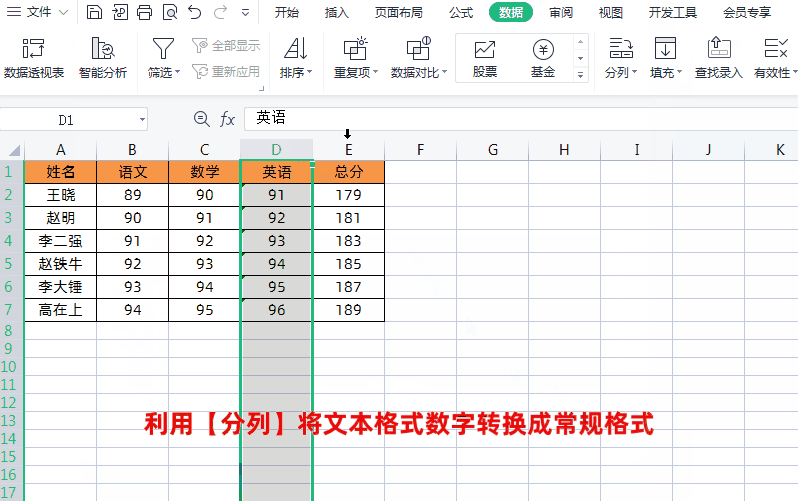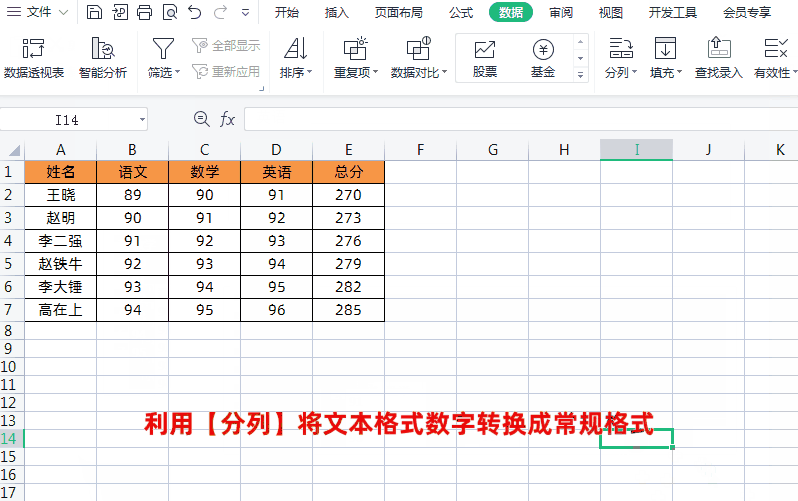
方法3将文本格式转换成常规格式求和我们可以通过选中每列数据→点击【数据】→【分列】→【完成】,将文本格式数字转换成常规格式,这样就可以正常进行求和运算了,如下图所示
以上是【桃大喵学习记】今天的干货分享~觉得内容对你有帮助,记得顺手点个赞哟~。我会经常分享职场办公软件使用技巧干货!大家有什么问题欢迎留言关注!
亲爱的读者们,感谢您花时间阅读本文。如果您对本文有任何疑问或建议,请随时联系我。我非常乐意与您交流。







发表评论:
◎欢迎参与讨论,请在这里发表您的看法、交流您的观点。